
CD8+T細(xì)胞是適應(yīng)性免疫應(yīng)答的核心執(zhí)行者,在抗原刺激下,初始T細(xì)胞分化為效應(yīng)性T細(xì)胞以清除病原體或腫瘤細(xì)胞,其中少數(shù)細(xì)胞(<5%)進(jìn)一步分化為記憶性T細(xì)胞,為機(jī)體提供長(zhǎng)期免疫保護(hù)。這一過(guò)程伴隨顯著的代謝重塑,而NADPH作為細(xì)胞內(nèi)關(guān)鍵的還原力供體,在生物合成和氧化還原平衡中發(fā)揮重要作用。盡管氧化型磷酸戊糖途徑被認(rèn)為是NADPH的主要來(lái)源,非氧化型磷酸戊糖途徑在這一過(guò)程中的具體功能尚不清晰。
2026年2月20日,華中科技大學(xué)同濟(jì)醫(yī)學(xué)院基礎(chǔ)醫(yī)學(xué)院張華鋒教授團(tuán)隊(duì)與湖北醫(yī)藥學(xué)院附屬太和醫(yī)院楊卓順教授團(tuán)隊(duì)在PNAS雜志發(fā)表了題為《Non-oxidative pentose phosphate pathway regulates CD8+ T cell immunity by maintaining NADPH homeostasis》的最新研究成果。該研究系統(tǒng)闡明了非氧化磷酸戊糖途徑(non-oxidative pentose phosphate pathway, non-oxPPP)在CD8+T細(xì)胞活化、增殖及記憶形成過(guò)程中的功能與分子機(jī)制。
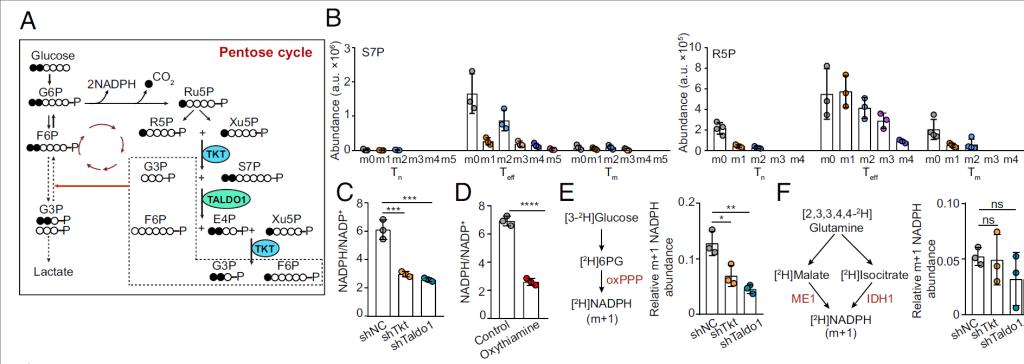
本研究團(tuán)隊(duì)早期的成果已證實(shí)CD8+記憶性T細(xì)胞中有大量的糖原儲(chǔ)存,糖原分解產(chǎn)生的6磷酸葡萄糖進(jìn)入磷酸戊糖途徑,產(chǎn)生還原型NADPH,維持高水平的還原性谷胱甘肽,及時(shí)清除細(xì)胞內(nèi)的自由基,從而維持記憶性T細(xì)胞的長(zhǎng)期存活(Nat Cell Biol.2018;20:21-27;Nat Cell Biol.2020;22:18-25;Mol Cell.2022;82:3077-3088.e6.)。在此基礎(chǔ)上,研究團(tuán)隊(duì)進(jìn)一步發(fā)現(xiàn),T細(xì)胞分化過(guò)程中,CD8+效應(yīng)性T細(xì)胞和記憶性T細(xì)胞中非氧化磷酸戊糖途徑的關(guān)鍵酶轉(zhuǎn)酮醇酶(TKT)和轉(zhuǎn)醛醇酶(TALDO1)的表達(dá)水平均上調(diào)。利用代謝組學(xué)和穩(wěn)定同位素示蹤技術(shù),團(tuán)隊(duì)證實(shí)活化的CD8+T細(xì)胞通過(guò)增強(qiáng)該途徑,形成了“戊糖循環(huán)”代謝模式。這一模式將代謝中間產(chǎn)物重新導(dǎo)向氧化磷酸戊糖途徑和糖酵解,從而持續(xù)、高效地生成NADPH。功能實(shí)驗(yàn)表明,通過(guò)基因敲低或小分子藥物抑制TKT或TALDO1,會(huì)導(dǎo)致CD8+T細(xì)胞內(nèi)NADPH水平下降、活性氧累積、脂質(zhì)合成受阻及線(xiàn)粒體結(jié)構(gòu)損傷,進(jìn)而削弱效應(yīng)性T細(xì)胞的增殖能力、細(xì)胞因子產(chǎn)生及體內(nèi)抗腫瘤功能。在記憶性T細(xì)胞分化過(guò)程中,抑制該通路同樣導(dǎo)致記憶前體細(xì)胞比例下降、記憶性T細(xì)胞長(zhǎng)期維持能力減弱,再次遭受抗原刺激時(shí)二次應(yīng)答功能受損。
研究進(jìn)一步發(fā)現(xiàn),增強(qiáng)非氧化磷酸戊糖途徑活性雖然不影響CD8+效應(yīng)性T細(xì)胞的功能,但可促進(jìn)CD8+記憶性T細(xì)胞的分化與長(zhǎng)期維持,并在腫瘤模型中表現(xiàn)出更好的抗腫瘤效應(yīng)。機(jī)制研究表明,該途徑主要通過(guò)維持NADPH穩(wěn)態(tài)、調(diào)控細(xì)胞內(nèi)氧化還原狀態(tài)來(lái)支持記憶性T細(xì)胞的存活與功能。在腫瘤過(guò)繼治療模型中,增強(qiáng)TKT或TALDO1表達(dá)可提高過(guò)繼CD8+T細(xì)胞在腫瘤微環(huán)境中的存活率和功能持久性,提示非氧化磷酸戊糖途徑可能成為改善T細(xì)胞免疫治療的新靶點(diǎn)。
綜上所述,該研究揭示了非氧化型磷酸戊糖代謝通路通過(guò)調(diào)控NADPH穩(wěn)態(tài),整合能量代謝、氧化還原平衡和生物合成的調(diào)控模式和分子機(jī)制,為理解CD8+T細(xì)胞的代謝基礎(chǔ)提供了新視角。
華中科技大學(xué)同濟(jì)醫(yī)學(xué)院基礎(chǔ)醫(yī)學(xué)院博士生馮京宇、張倩為共同第一作者,張華鋒教授和楊卓順教授為共同通訊作者。華中科技大學(xué)基礎(chǔ)醫(yī)學(xué)院為第一完成單位。研究得到中國(guó)醫(yī)學(xué)科學(xué)院基礎(chǔ)醫(yī)學(xué)研究所黃波教授大力支持。本研究得到國(guó)家自然科學(xué)基金等項(xiàng)目的資助。
原文鏈接:https://doi.org/10.1073/pnas.2526325123

 學(xué)院官方微信
學(xué)院官方微信